Како именовати хемијска једињења
Аутор:
Laura McKinney
Датум Стварања:
2 Април 2021
Ажурирати Датум:
26 Јуни 2024

Садржај
- фазе
- Метода 1 Номенклатура јонских једињења
- Метода 2 Номенклатура полиатомских једињења
- Метода 3 Номенклатура ковалентних једињења
Успех у области хемије захтева знање како именовати основна хемијска једињења. Овај водич вам пружа основна правила о поступку именовања хемијских једињења и како доделити имена једињењима која вам нису позната.
фазе
Метода 1 Номенклатура јонских једињења
- Шта је јонско једињење? Јонска једињења састоје се од метала и неметала. Затим погледајте Периодну табелу елемената да бисте сазнали које категорије припадају елементима присутним у једињењу.
-

Обликујте име. Ништа лакше од именовања јонског једињења два елемента. Заиста, први део имена једињења одговара називу неметалног елемента који носи суфикс "уре", док други одговара имену металног елемента. Постоје изузеци: оксид, фосфид, нитрид, сулфид.- Пример: Ал2о3. ал2 = Алуминијум; о3 = Кисеоник. Дакле, назив једињења биће „алуминијум оксид“.
-
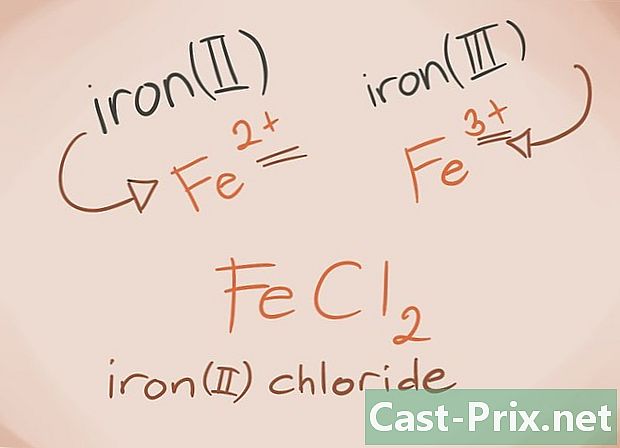
Знајте прелазне метале Прелазни метали су они који се налазе у Д и Ф блоковима периодичне табеле. На име једињења, набој на тим металима написан је римским бројевима. То је зато што прелазни метали могу да носе веће оптерећење и да формирају више једињења.- Пример: ФеЦл2 и ФеЦл3. Фе = гвожђе; цл2 = -2 хлорид; цл3 = Хлорид -3. Као имена ће се наћи железов хлорид (ИИ) и железов хлорид (ИИИ).
Метода 2 Номенклатура полиатомских једињења
-

Морате да схватите шта је полиатомско једињење. Полиатомска једињења су једињења која су формирана групом датома повезаних међусобно; цела група која носи набој је позитивна или негативна. Постоје три основне акције које можете вршити на полиатомским једињењима:- Првом делу једињења можете додати водоник. Реч "водоник" заиста се додаје на почетку имена једињења. Ово ће смањити вредност негативног наелектрисања за један. На пример, "карбонатни" ЦО3 постаје ХЦО "хидрогенкарбонат"3.

- Такође можете да уклоните кисеоник из једињења. Оптерећење се не мења, али "-ате" суфикс једињења се мења у "-икуе". На пример трансформација: НО3 у НЕ2 прелазимо из нитрата у нитрат. "

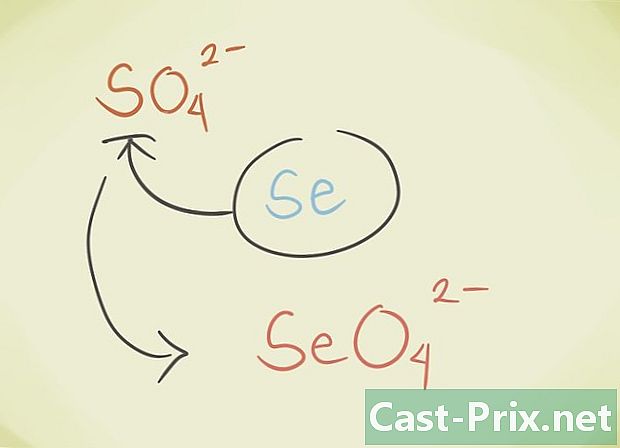
- Можете заменити централни латоме једињења са другим атомом који припада истој периодичној групи. На пример, СО сулфат4 може заменити Селенате СеО4.
- Првом делу једињења можете додати водоник. Реч "водоник" заиста се додаје на почетку имена једињења. Ово ће смањити вредност негативног наелектрисања за један. На пример, "карбонатни" ЦО3 постаје ХЦО "хидрогенкарбонат"3.
-

Запамтите најчешће дионске групе. Доње групе се користе за формирање већине полиатомских једињења. Пратећи редослед њиховог негативног набоја, имамо:- хидроксидни јони: ОХ
- нитратни јони: НО3
- Јони водоник-карбоната: ХЦО3
- перманганатни јони: МнО4
- карбонатни јони: ЦО3
- хроматни јони: ЦрО4
- дихроматни јони: Цр2о7
- сулфатни јони: СО4
- сулфитни јони: СО3
- тиосулфатни јони: С2О3
- Фосфатни јони: ПО4
- амонијум јони: НХ4
- С горње листе формирајте имена сложених састојака. Формирајте називну везу са било којом ставком која се односи на групу. Ако се елемент постави испред ионске групе, тада ће се име елемента једноставно додати на име сложеног дела.
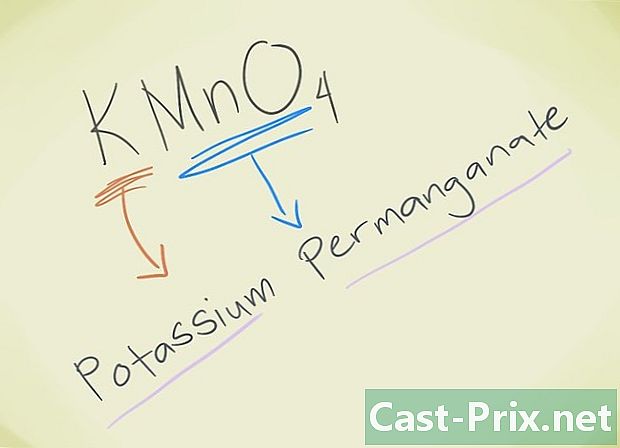
- Пример: КМнО4. Морате бити у стању да знате тог лава МнО4 одговара лавовом перманганату. К се односи на калијум. Дакле, ваше једињење ће се назвати перманганат калијум.
- Пример: НаОХ. Вероватно сте овде схватили да је то ОХОХ. На је натријум, па ће се једињење звати натријум хидроксид.

- Пример: КМнО4. Морате бити у стању да знате тог лава МнО4 одговара лавовом перманганату. К се односи на калијум. Дакле, ваше једињење ће се назвати перманганат калијум.
Метода 3 Номенклатура ковалентних једињења
-
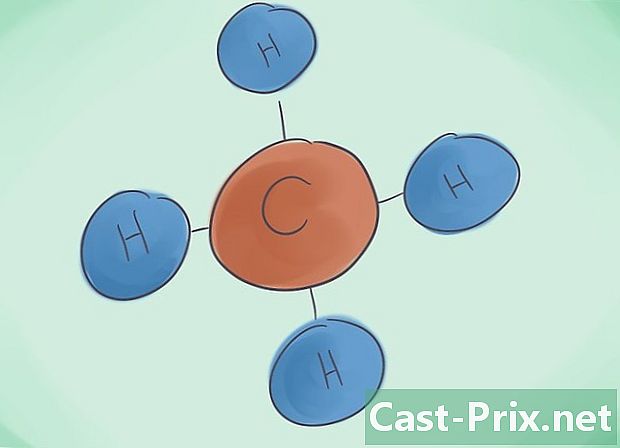
Шта је ковалентно једињење? Ковалентна једињења су резултат удруживања најмање два неметална елемента. Назив једињења одређује се бројем датома који га чине. Грчки префикс поред овог имена означава број молекула присутних у једињењу. -
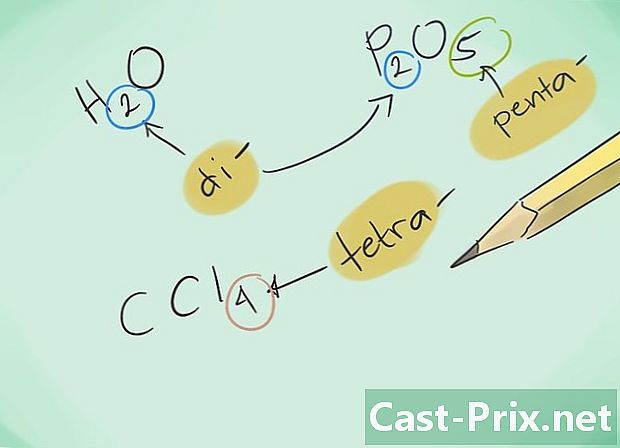
Упознајте се са префиксима. Запамтите следеће префиксе за једињења од 1 до 8 атома:- 1 атом - "Моно-"
- 2 атома - "Ди-"
- 3 атома - "Три-"
- 4 атома - "Тетра-"
- 5 атома - "Пента-"
- 6 атома - "Хекса-"
- 7 атома - "Хепта-"
- 8 атома - "окта-"
- Затим наведите једињења. Наведите добијени спој користећи одговарајуће префиксе. Префикси се цепију на сваки од елемената који чине једињење са неколико атома.
- Пример: ЦО ће се вратити у угљен моноксид док ЦО2 ће означавати угљендиоксид.
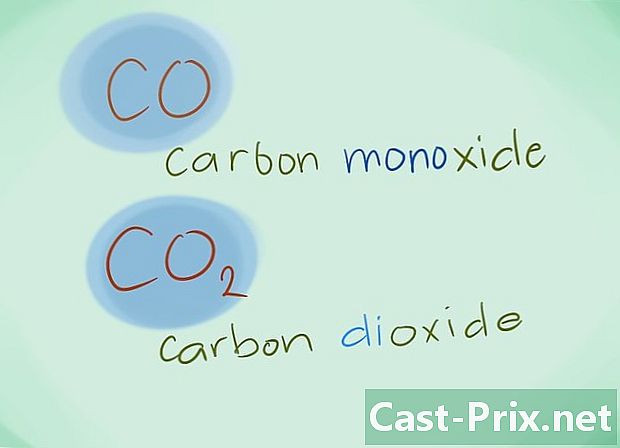
- Пример: Н2Н3 одговарао би азотном трисулфиду.

- У већини случајева, префикс „моно“ може бити изостављен; ово, више него било који недостатак префикса, подстиче да се потоњи треба користити. Овај префикс се и даље користи у случају угљен-моноксида с обзиром на чињеницу да ова употреба сеже до првих хемијских трагова.
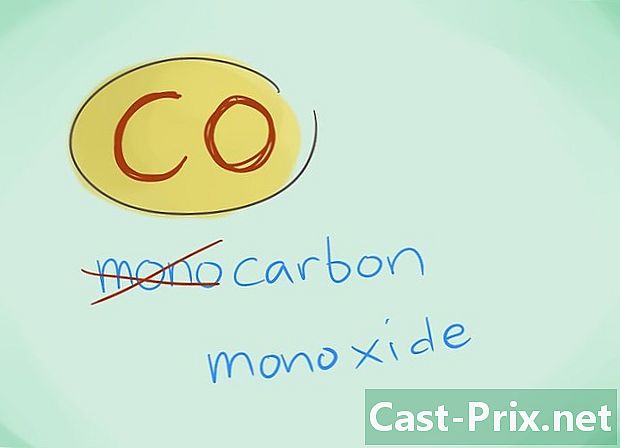
- Пример: ЦО ће се вратити у угљен моноксид док ЦО2 ће означавати угљендиоксид.
- Наравно, сумњате да се на сва ова правила примјењује неколико изузетака; задржите на пример ову формулу, ЦаЦл2Очекујете да ћете га назвати „калцијумовим дихлоридом“, што је НЕ. Ваше једињење ће једноставно задржати назив калцијум хлорид.
- Такође треба напоменути да се све ово не односи на органску хемију.
- Детаљна правила овде су намењена почетничкој публици из хемије и науке. Врло су различита правила када прођете кроз напредни ниво хемије, попут правила о променљивој валенцији.

